2017年8月16日��,來自德國(guó)馬克斯普朗克感染生物學(xué)研究所的Thomas F. Meyer博士和美國(guó)斯坦福大學(xué)醫(yī)學(xué)院的研究人員合作首次發(fā)現(xiàn)了幽門螺桿菌導(dǎo)致胃癌的可能機(jī)制。他們發(fā)現(xiàn)�����,幽門螺桿菌感染可能通過誘導(dǎo)胃粘膜下方干細(xì)胞的過度增殖���,致使干細(xì)胞在增殖過程中積累大量的DNA損傷�,從而誘導(dǎo)癌癥的發(fā)生�����。這一發(fā)現(xiàn)發(fā)表在《自然》雜志上(1)�����。

Meyer博士
1875年�����,德國(guó)一些學(xué)者首次在人體的胃中發(fā)現(xiàn)了一種螺旋細(xì)菌,但因無法在容器中培植��,研究結(jié)果并沒有受到太大的重視(2)�����。直到一個(gè)世紀(jì)之后���,1982年�����,兩名來自澳大利亞的科學(xué)家,魯賓·華倫和巴利·馬歇爾再次分離出該種細(xì)菌��,并發(fā)現(xiàn)這一細(xì)菌是導(dǎo)致胃潰瘍的“元兇”�,才讓人們對(duì)幽門螺旋桿菌產(chǎn)生了狂熱興趣。這一發(fā)現(xiàn)于1983年發(fā)表在《柳葉刀》雜志上(3)�。二人也因此獲得了2005年的諾貝爾生理學(xué)和醫(yī)學(xué)獎(jiǎng)。

2005年諾貝爾獎(jiǎng)?lì)C獎(jiǎng)晚會(huì)上魯賓·華倫和巴利·馬歇爾博士
而隨后的大量研究發(fā)現(xiàn)���,幽門螺桿菌不僅可以通過感染胃粘膜細(xì)胞����,引起胃潰瘍,也和胃癌發(fā)生密切相關(guān)���。例如��,1991年《新英格蘭醫(yī)學(xué)》雜志上發(fā)表的一項(xiàng)研究表明�,60%的胃腺癌可以歸因于幽門螺旋桿菌感染(4)�����。因此����,在1994年,幽門螺桿菌也被世界衛(wèi)生組織列為一級(jí)致癌物(對(duì)人體有明確致癌性的物質(zhì)或混合物���,如黃曲霉素���,砒霜等等)(5)。
在我國(guó)�,幽門螺桿菌的總體流行率還是很高的。根據(jù)2002年-2004年對(duì)我國(guó)19個(gè)省市自治區(qū)一般人群26341人進(jìn)行的一項(xiàng)流行病學(xué)調(diào)查發(fā)現(xiàn)�����,我國(guó)的幽門螺桿菌的總感染率超過56%,其中廣東地區(qū)最低為42%����,西藏最高為84.6%(6)。也就是說����,在我國(guó)平均每?jī)蓚€(gè)人中就有一個(gè)人感染了幽門螺桿菌。
同時(shí)��,根據(jù)世界衛(wèi)生組織2014年的統(tǒng)計(jì)資料�����,我國(guó)胃癌死亡人數(shù)占全球胃癌死亡人數(shù)的比例高達(dá)47%(7)�����。也就是說�,全球近一半的胃癌患者死亡發(fā)生在我們國(guó)家�。
雖然,人們發(fā)現(xiàn)幽門螺桿菌感染與胃癌的發(fā)生密切相關(guān)�,但是與致癌病毒不同�����,細(xì)菌不會(huì)將致癌基因轉(zhuǎn)入宿主細(xì)胞內(nèi)�����。因此���,在此之前,人們并不清楚幽門螺桿菌是如何誘導(dǎo)胃癌發(fā)生的�。
之前,馬克斯普朗克的臨床學(xué)家Michael Sigal就已經(jīng)發(fā)現(xiàn)��,幽門螺桿菌不僅僅只會(huì)感染胃粘膜表面的細(xì)胞����,而且還會(huì)侵入到胃粘膜深部,達(dá)到干細(xì)胞池��。同時(shí)���,Sigal還觀察到���,這些干細(xì)胞還會(huì)通過增加其分裂來對(duì)感染做出反應(yīng)(8)�。是不是這個(gè)過程導(dǎo)致了胃癌�?那具體機(jī)制又是什么呢?
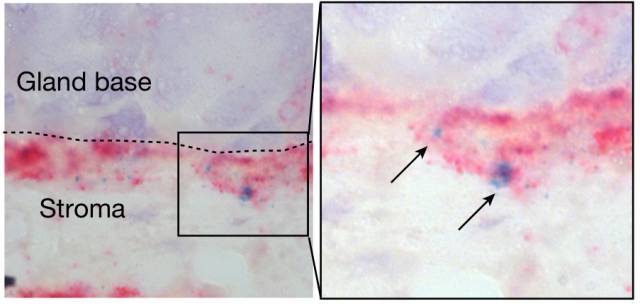
干細(xì)胞位于胃腺的底部��,受基質(zhì)成纖維細(xì)胞釋放的R-脊髓蛋白蛋白(箭頭)調(diào)節(jié)增殖活性
已有研究表明���,在正常干細(xì)胞增殖過程中�����,DNA復(fù)制過程中產(chǎn)生的隨機(jī)突變是一種強(qiáng)烈的致癌因素����,超過遺傳以及環(huán)境因素等(9)�����。因此��,幽門螺桿菌很有可能是通過促進(jìn)胃粘膜干細(xì)胞的過度增殖��,引起大量DNA損傷����,最終誘導(dǎo)胃癌的發(fā)生。
為了確定幽門螺桿菌具體是如何促進(jìn)胃粘膜干細(xì)胞增殖的����。Meyer博士采用單分子原位雜交技術(shù)對(duì)小鼠胃粘膜干細(xì)胞進(jìn)行系統(tǒng)分析。結(jié)果發(fā)現(xiàn)�����,小鼠的胃粘膜下���,位于胃腺基底的干細(xì)胞池中存在兩種不同類型的干細(xì)胞��。一種干細(xì)胞分化程度低�,增殖能力強(qiáng)�,另一種分化程度較高,增殖能力較弱���。
同時(shí)�,Meyer博士還發(fā)現(xiàn)���,當(dāng)幽門螺桿菌侵入時(shí)�,胃粘膜下方的間質(zhì)成纖維細(xì)胞會(huì)分泌一種名為R-脊髓蛋白(Rspo)的物質(zhì),作用于胃粘膜下方干細(xì)胞池���,激活干細(xì)胞的WNT通路調(diào)節(jié)干細(xì)胞的增殖以應(yīng)對(duì)幽門螺桿菌感染����。
但是�����,Meyer博士發(fā)現(xiàn)�,這兩種細(xì)胞對(duì)WNT通路的反應(yīng)是不同的。正常Rspo作用于分化程度低����,增殖較快的干細(xì)胞在后,會(huì)使干細(xì)胞的增殖速度顯著加快�,導(dǎo)致其過度增殖。而Rspo作用于增殖較慢的細(xì)胞后�����,會(huì)顯著抑制其增殖�。
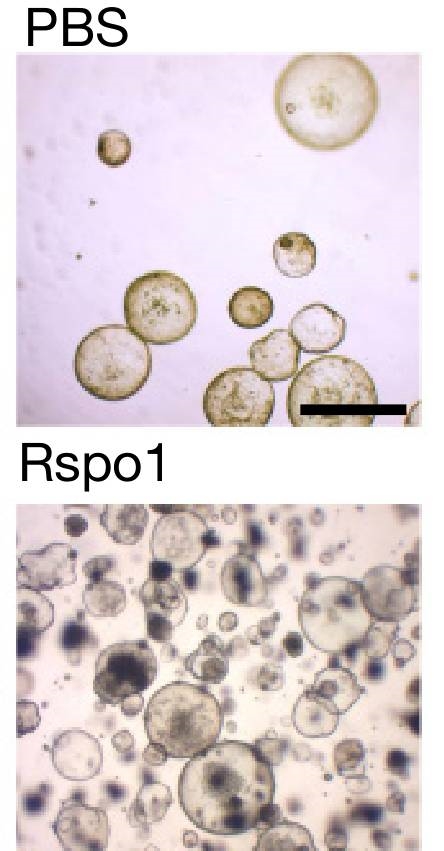
Rspo會(huì)顯著增強(qiáng)敏感干細(xì)胞的擴(kuò)增速度(單細(xì)胞培養(yǎng)24小時(shí))
正如Sigal博士所說,“由于幽門螺桿菌引起感染機(jī)體無法自我治愈���,因此��,若不治療����,幽門螺桿菌可能長(zhǎng)期持續(xù)刺激間質(zhì)成纖維細(xì)胞分泌Rspo來刺激干細(xì)胞分裂�,這也許足以解釋為什么幽門螺桿菌感染會(huì)顯著增加胃癌風(fēng)險(xiǎn)(10)。”
總的來說�����,Meyer博士的研究揭示了慢性細(xì)菌感染是如何干擾組織的功能的��,并提供了關(guān)于幽門螺桿菌如何增加胃癌風(fēng)險(xiǎn)的首個(gè)寶貴線索�。而我國(guó)人口基數(shù)大,幽門螺桿菌的感染率高����,這也是我國(guó)胃癌發(fā)病人數(shù)以及死亡人數(shù)如此之高的可能原因。而此前的研究表明���,進(jìn)行幽門螺桿菌根治治療可以減少65%的胃癌風(fēng)險(xiǎn)(11)���。因此,為了減少胃癌的發(fā)生,感染者還是應(yīng)該盡早接受幽門螺桿菌根除治療��。
參考資料:
1.http://www.nature.com/nature/journal/vaop/ncurrent/full/nature23642.html?foxtrotcallback=true
2.https://www.nature.com/scientificamerican/journal/v292/n2/full/scientificamerican0205-38.html
3.Warren JR, Marshall BJ. Unidentifi ed curved bacilli on gastric epithelium in active chronic gastritis. Lancet 1983;I:1273–5.
4.Parsonnet J, Friedman G D, Vandersteen D P, et al. Helicobacter pylori infection and the risk of gastric carcinoma[J]. New England Journal of Medicine, 1991, 325(16): 1127-1131.
5.IARC. Working Group on the Evaluation of Carcinogenic Risks to Humans. Helicobacter pylori. In: Schistosomes, liver fl ukes and Helicobacter pylori views and expert opinions of an IARC Working Group On The Evaluation of Carcinogenic Risks To Humans. Lyon: IARC 1994. p. 177–240.
6.張萬岱, 胡伏蓮, 蕭樹東, 等. 中國(guó)自然人群幽門螺桿菌感染的流行病學(xué)調(diào)查[J]. 現(xiàn)代消化及介入診療, 2010, 15(5): 265-270.
7.Stewart B, Wild C P. World cancer report 2014[J]. Health, 2017.
8.Sigal, M. et al. Helicobacter pylori activates and expands Lgr5+ stem cells through direct colonization of the gastric glands. Gastroenterology 148, 1392–404.e21 (2015).
9.Tomasetti C, Vogelstein B. Variation in cancer risk among tissues can be explained by the number of stem cell divisions[J]. Science, 2015, 347(6217): 78-81.
10.https://www.mpg.de/11437780/stomach-cancer-helicobacter-pylori-infection
11.Fuccio L, Zagari R M, Eusebi L H, et al. Meta-analysis: can Helicobacter pylori eradication treatment reduce the risk for gastric cancer?[J]. Annals of internal medicine, 2009, 151(2): 121-128.